Ernst-Jan Eggers1,2, Ate van der Burgt1, Sjaak AW van Heusden2, Michiel E. de Vries@ 1, Richard GF Visser©2, Christian WB Bachem©2и & Pim Lindhout1
Fitimi gjenetik në patate pengohet nga gjenomi tetraploid heterozigot i patates së kultivuar. Shndërrimi i patates në një kulture hibride F1 të bazuar në linjën diploide inbred ofron një rrugë premtuese drejt rritjes së përfitimit gjenetik. Futja e një gjeni mbizotërues të frenuesit të S-lokusit (Sli) në germplazmën diploide të patates lejon gjenerimin efikas të farave të vetë-fertilizuara dhe në këtë mënyrë zhvillimin e linjave inbred të patates. Dihet pak për strukturën dhe funksionin e vendndodhjes Sli. Këtu ne përshkruajmë hartëzimin e Sli në një interval 12.6 kb në kromozomin 12 duke përdorur një qasje të ekranit rekombinant. Një nga dy gjenet kandidate të pranishme në këtë interval tregon një sekuencë unike që është ekskluzivisht e pranishme në linja të vetë-përputhshme. Ne përshkruajmë një vektor shprehjeje që konverton veten të papajtueshëm gjenotipet në vetë-përputhshmëri dhe një vektor CRISPR-Cas9 që konverton gjenotipet SC në SI. Gjeni Sli kodon një proteinë F-box që shprehet në mënyrë specifike në polen nga bimët e vetë-përputhshme. Një futje prej 533 bp në promotorin e atij gjeni çon në një fitim të mutacionit të funksionit, i cili kapërcen refuzimin e vetëpolenit.
Patatja është kultura më e rëndësishme ushqimore pa drithëra në botë. Megjithatë, ndërsa kulturat e tjera ushqimore si misri, orizi dhe gruri kanë treguar një rritje gjenetike të rendimentit prej 1% në vit1, fitimi gjenetik në patate ka qenë minimal2. Aktualisht, shumica e kultivarëve të patateve të rritura komercialisht rrjedhin nga kryqëzimet midis prindërve autotetraploidë heterozigotë. Në këtë sistem mbarështimi, qindra mijëra fidanë gjenerohen dhe ekzaminohen në çdo brez mbarështues për të identifikuar ata individë të rrallë që kanë karakteristika të pranueshme për tipare të shumta që ndahen në pasardhës. Meqenëse ka rreth pesëdhjetë tipare që janë të rëndësishme për vlerën e një kultivari komercial të patates, mundësia për të kombinuar alelët më të mirë që kontrollojnë këto tipare duke përdorur mbarështimin konvencional të patates është e papërfillshme. Përveç kësaj, futja e synuar e tipareve të reja në kultivarët elitë duke ruajtur integritetin gjenetik nëpërmjet skemave të kryqëzimit është e pamundur pa linja prindërore homozigote. Për të kapërcyer këto probleme, disa grupe kanë filluar programet e mbarështimit të patateve diploide të bazuara në linjën e brendshme.2-5. Në këto programe, përfitimet gjenetike arrihen nëpërmjet përmirësimeve në rritje të linjave prindërore duke përzgjedhur vazhdimisht kundër aleleve të dëmshme gjatë bashkimit të gjakut dhe duke grumbulluar alele të dobishme në linjat inbred përmes skemave të kryqëzimit të pasme.6. Linjat e brendshme prindërore më pas kryqëzohen për të prodhuar pasardhës heterotikë hibridë F1.
Në shumicën e gjenotipeve diploide të patates, gjakderdhja është shumë e kufizuar nga një sistem i vetë-papajtueshmërisë gametofitike (GSI) që kontrollohet nga lokusi S multi-alelik. Ky S-lokus kodon S-RNaza të shprehura në stil që pengojnë rritjen e tubit të vetë-polenit në stil, duke parandaluar vetëfertilizimin7. Gjatë pjalmimit të kryqëzuar, proteinat S-lokus F-box (SLF) të shprehura me polen njohin S-RNases dhe i synojnë ato në rrugën e degradimit proteazomal, duke lejuar rritjen e tubit të polenit drejt vezoreve ku mund të ndodhë fekondimi.8. Çdo S-alele kodon një S-RNase dhe SLF të shumta me specifika të ndryshme, të cilat së bashku mund të njohin të gjitha S-RNase përveç S-RNazës që është e pranishme në të njëjtin alel.9.
Edhe pse shumica e linjave të patates diploide janë të vetë-papajtueshme (SI), linjat e vetë-përputhshme të patates ekzistojnë dhe mund të përdoren për të futur vetë-përputhshmërinë në programet e mbarështimit të patates diploide10-12. Hosaka dhe Hanneman hartuan një frenues dominues të S-lokusit (Sli) gjen nga a Solanum chacoense u ngjit në skajin distal të kromozomit 12 dhe e përdori atë për të gjeneruar linja të brendshme të patates13'14. Bazuar në rezultatet e tyre, Hosaka dhe Hanneman sugjeruan këtë Rrëshqitje është një gjen i shprehur në polen me veprim sporofit dhe atë homozigozitet për Rrëshqitje është vdekjeprurëse pasi homozigot SliSli gjenotipet mungonin në popullatën F8 të S. kakoense. Ne përdorëm një nga këto S. kakoense Linjat inbred që rrjedhin nga (DS) për të futur vetë-përputhshmërinë në S. tuberozë prejardhje. Këtu, ne përshkruajmë identifikimin e gjenit shkakësor të vetëpërputhshmërisë për të fituar njohuri të mëtejshme në biologjinë e vetëpërputhshmërisë në patatet diploide.
Rezultate dhe diskutime
Në një popullatë F2 që rrjedh nga një kryqëzim ndërmjet Rrëshqitje donator (i caktuar DS) dhe një diploid S. tuberozë (D2) ne vëzhguam një QTL me efekt modest për grupin e vetë-manaferrave në kromozomin 2, por një shqyrtim i mëvonshëm rekombinant nuk ishte i suksesshëm. Ne vumë re se popullata të shumta F2 treguan anshmëri ekstreme rreth krahut të gjatë të kromozomit 12, me homozigozitetin për haplotipin jo-DS që mungonte plotësisht.
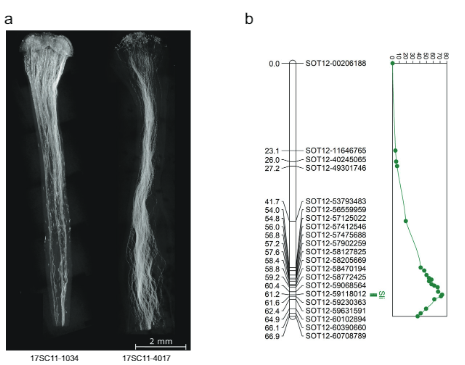
Bazuar në këtë anshmëri dhe në hartëzimin e Rrëshqitje në kromozomin 12, ne hipotezuam se Rrëshqitje shprehet në mënyrë gametofitike, që do të thotë se në një vetëpllenim të një bime heterozigote për Rrëshqitje (Sli/sli), vetëm polen që përmban dominantin Rrëshqitje aleli mund të marrë pjesë në vetëfertilizimin. Për të testuar këtë hipotezë, ne kaluam një linjë të fuqishme dhe shumë vetë-pjellore (16HP1-66) në një linjë të fuqishme të vetë-papajtueshme (D16), sekuencuam të dyja me gjenomin e plotë dhe analizuam popullatën F1 që rezulton (17SC11, n = 251, Fig. 1a, b). Meqenëse kjo popullatë F1 është shumë polimorfike për shumë lokuse, ne vëzhguam një gamë të gjerë fenotipësh, duke përfshirë ato që lidhen me fertilitetin. Prandaj, ne kemi zbatuar një protokoll shumë të rreptë dhe rigoroz të fenotipizimit që përfshin grupin e frutave dhe farave si nga pjalmimet kryq ashtu edhe nga vetëpjalmimi, si dhe vizualizimi i rritjes së tubit të polenit në stile për të shmangur çështjet e sterilitetit që ngatërrojnë fenotipin e përputhshmërisë. Bimët që vendosin më shumë se një kokrra të kuqe konsiderohen SC, ndërsa bimët që nuk vendosin kokrra të kuqe pas të paktën 10 vetëpjalmimesh, tregojnë ndalim të rritjes së tubit të vetë-polenit në stilin dhe vendosin kokrra të kryqëzuara pas pjalmimit me masë. poleni konsiderohen SI. Si rezultat, një pjesë e konsiderueshme e popullsisë u përjashtua nga analizat gjenetike pasi kërkesat për të vlerësuar në mënyrë të qartë fenotipin e përputhshmërisë nuk u plotësuan. Megjithatë, statusi i përputhshmërisë së shumicës së pasardhësve të popullsisë 17SC11 mund të vlerësohej dhe u tregua se ndahej për vetë-përputhshmëri (Të dhënat Suplementare 1). Meqenëse vetë-përputhshmëria ka origjinën nga 16HP1-66, ne përdorëm të gjithë sekuencat e gjenomit të këtij gjenotipi për të dizajnuar shënuesit KASP që synojnë SNP në kromozomet 2 dhe 12 që janë heterozigotë në 16HP1-66, por homozigotë në D16, duke mundësuar hartimin e Rrëshqitje në mejozën e nënës. Ne ndërtuam një hartë gjenetike, kryem analizën QTL dhe gjetëm një QTL shumë domethënëse (LOD = 75.72) në krahun e gjatë të kromozomit 12 (Fig. 1b), duke konfirmuar rezultatet e Hosaka dhe Hanneman.
Për të konfirmuar QTL-në në një sfond gjenetik të ndryshëm, ne kaluam një tjetër gjenotip shumë vetë-pjellor që rrjedh nga programi i mbarështimit Solynta me gjenotipin SI D14 dhe analizuam popullatën F1 që rezulton (17SC25, Të dhëna Suplementare 1). Midis 32 individëve të popullsisë 17SC25, nuk gjetëm individë SI. Për të gjeneruar një popullsi të veçuar, ne zgjodhëm gjenotipin më pjellor dhe e kaluam atë në dy gjenotipe SI që identifikuam në popullatën 17SC11, duke rezultuar në popullatat 18SC11 dhe 18SC12 (Të dhënat Suplementare 1 dhe Fig. Suplementare 1). Siç pritej, analiza e popullatave 18SC11 dhe 18SC12 tregoi se të dyja popullatat ndahen për vetë-përputhshmëri. Ne dërguam nënën (17SC25-8) për sekuencën e plotë të gjenomit dhe përdorëm këto të dhëna për të dizajnuar shënues të rinj KASP duke përdorur të njëjtën qasje si ajo e përdorur për popullatën 17SC11, por këtë herë duke synuar vetëm kromozomin 12. Analiza e mëvonshme QTL konfirmoi QTL-në që gjetëm në popullatë 17SC11 me vlera LOD prej 33.14 dhe 120.94 në popullatat 18SC11 dhe 18SC12, përkatësisht (Fig. Suplementare 2).
Për të përcaktuar nëse Rrëshqitje është me të vërtetë e shprehur në mënyrë gametofitike, ne analizuam një popullatë F2 (19SC1, n = 160) rrjedh nga një individ pjellor dhe i fuqishëm 17SC11. Lulëzimi dhe fertiliteti në këtë popullatë u reduktuan në krahasim me F1. Në analizën fenotipike, nga 160 bimë, 81 bimë ishin të vetë-përputhshme, 78 u kategorizuan si të papërcaktuara (ND) për shkak të lulëzimit të dobët ose pjellorisë së dobët dhe një bimë u vlerësua e vetë-papajtueshme (Të dhënat Suplementare 1). Ne projektuam shënuesit KASP që synojnë SNP në kromozomin 12 që janë homozigotë për alelet alternative te prindërit 16HP1-66 dhe D16. Përgjatë gjithë raporteve të ndarjes së kromozomit 12 devijojnë ndjeshëm nga ndarja e pritur 1:2:1. Për më tepër, rreth QTL-së së vetëpërputhshmërisë, nuk ka lokacione homozigote për haplotipin e prindit D16 (Fig. 3 plotësuese), duke treguar në vend të kësaj një ndarje 1:1 për heterozigot D16/16HP1-66: homozigotë 16HP1-66, duke sugjeruar që eliminimi i mungon poleni Rrëshqitje shkakton shtrembërim të segregacionit. Kjo mbështet hipotezën se vetëm poleni mban mbizotëruesin Rrëshqitje aleli marrin pjesë në vetëfertilizimin. Përveç kësaj, përveç një individi, fenotipizimi ishte përfundimtar për kontrastin midis SI dhe SC, duke treguar se protokolli i përdorur i fenotipizimit është i fortë dhe pothuajse pa gabime.
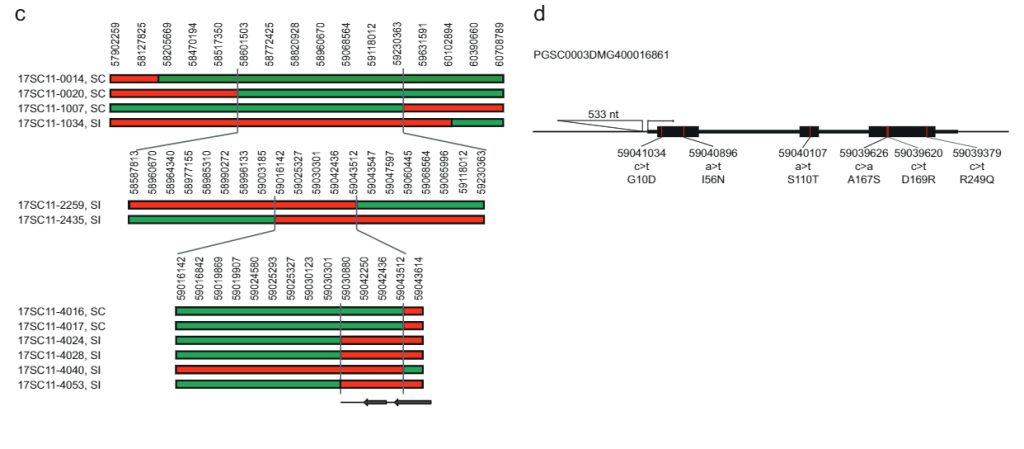
Ndërsa 628 KB SLI intervali në kromozomin 12 që mbante alelën Sli nga popullata 17SC11 u reduktua në një interval më të vogël mbivendosjeje prej 169 KB në popullatën 18SC12, këto intervale ishin ende shumë të mëdha për të identifikuar gjenin Sli. Prandaj, ne synuam të reduktonim intervalin që përmban S/i nëpërmjet një qasjeje të shqyrtimit rekombinant. Për të identifikuar bimët me një rikombinim në Rrëshqitje interval, ne kemi gjenotipizuar 1374 fidanë 17SC11 me dy markera KASP në kufirin proksimal dhe dy në kufirin distal. Ne identifikuam 81 fidanë me rikombinim midis dy shënuesve më të jashtëm dhe zgjodhëm ato për hartimin e mëtejshëm të imët. Për të marrë fenotipe të paqarta, ne i shumuam në mënyrë vegjetative këto gjenotipe dhe kryem fenotipizimin në të paktën dy klone për gjenotip. Ne gjenotipuam 81 rekombinantë me më shumë shënues në interval dhe identifikuam dy rekombinantë informues që reduktuan intervalin në 27.37 KB që përmbanin pesë gjene të shënuar (Të dhënat Suplementare 1).
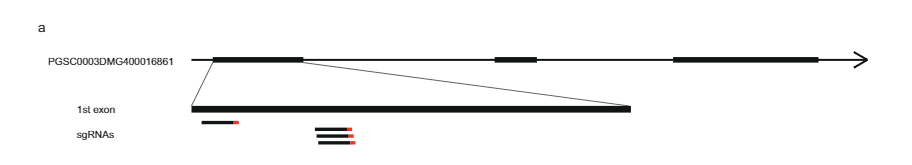
Për të reduktuar më tej intervalin, ne ekzaminuam 10165 fidanë të tjerë nga e njëjta popullatë me katër shënues rreth këtij intervali prej 27.37 KB dhe identifikuam 12 rekombinantë. Këta u gjenotipuan më tej me 14 shënues të tjerë në këtë interval dhe ne identifikuam gjashtë rekombinantë informues që treguan fenotipe të qarta përputhshmërie. Dy rekombinantë me një fenotip SC dhe një me një fenotip SI konfirmuan kufirin distal të intervalit 27.37 KB, ndërsa tre rekombinantë me një fenotip SI përcaktuan një kufi të ri proksimal që redukton intervalin në vetëm 12.6 kb që përmban dy gjene, PGSC0003DM400016861DM (PGSC0003DM400016860DDMXNUMXDM) Fik. 1c).
Për të identifikuar gjenin kandidat që është përgjegjës për fenotipin e vetëpërputhshëm, ne analizuam variacionin e sekuencës për këto dy gjene në disa linja të sekuencës së plotë të gjenomit diploid të patates (Të dhënat Suplementare 2). Duke krahasuar këtë variacion të sekuencës me fenotipet SC/SI të këtyre linjave, ne identifikuam të gjitha SNP-të specifike të SC dhe INDELS (Të dhënat Suplementare 2). Më pas, ne identifikuam manualisht të gjitha SNP-të jo-sinonime dhe përcaktuam nëse zëvendësimet e aminoacideve janë të zakonshme ose unike për proteinat e ngjashme në Solanaceae. Gjeni kandidat PGSC0003DMG400016861 tregon gjashtë zëvendësime të aminoacideve specifike SC dhe veçanërisht, një futje 533 bp e vendosur në —108 bp nga kodoni fillestar, duke sugjeruar që aleli SC ka ndryshuar shprehjen në krahasim me alelin SI. Bazuar në këto studime gjenetike, ne hipotezuam se PGSC0003DMG400016861 është Rrëshqitje gjen
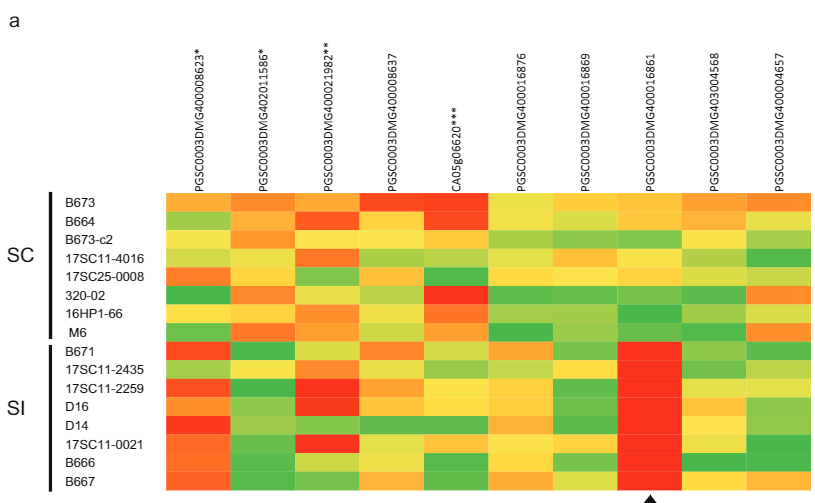
Për të verifikuar hipotezën se Sli shprehet në polen, ne mbirëm polen nga 10 gjenotipe patate SI dhe 10 SC in vitro dhe ekstraktuam ARN për renditjen e ARN-së. Nga dy gjenet e mbetura kandidate, u shpreh vetëm gjen kandidat PGSC0003DMG400016861, por ekskluzivisht në polen nga gjenotipet SC (Fig. 2a). Për më tepër, në bimët heterozigote për gjenin e supozuar kandidat Sli, u shpreh vetëm aleli Sli. Është interesante se gjene të tjera të shprehura me polen të vendosura afër vendndodhjes Sli në kromozomin 12 treguan nivele të ngjashme shprehjeje në bimët SC dhe SI (Fig. 2a). Prandaj, arritëm në përfundimin se vetëm gjeni PGSC0003DMG400016861 shprehet në mënyrë specifike në tubat e polenit të bimëve SC.
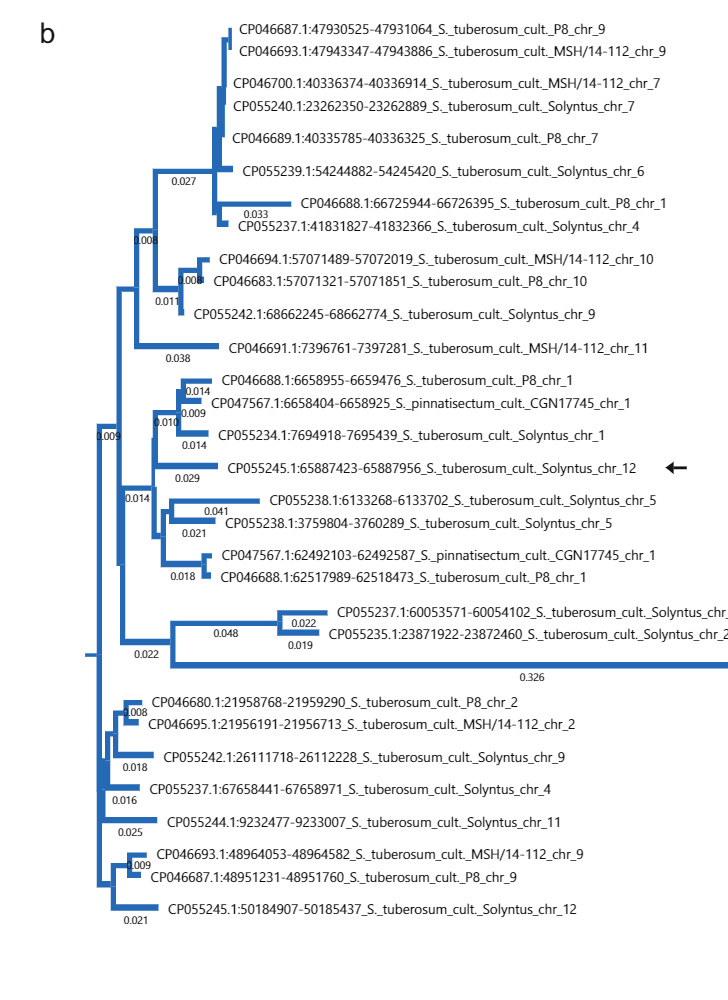
Për të hetuar origjinën e futjes 533 bp, ne kryem një kërkim BLAST të sekuencës 533 bp në NCBI. Është interesante se sekuencat jashtëzakonisht të ngjashme me futjen specifike të Sli janë të zakonshme në S të renditur. tuberozë aderimet (Fig. 2b). Për më tepër, futja 533 bp ka një homologji me një sekuencë në S. pennellii. Duke përdorur sekuencën nga S. pennellii si një pyetje BLAST ne gjetëm sekuenca të ngjashme në S. lycopersicum. Analiza filogjenetike e sekuencave në S. tuberosum, S. pennellii S. lycopersicum grupon S. pennellii sekuencë së bashku me S. lycopersicum dhe një S. tuberosum sekuencë, duke sugjeruar se këto kanë një origjinë të përbashkët (Fig. 4a plotësuese). Ne supozuam se futja rrjedh nga një element i transpozueshëm (TE). Ne krijuam një grafik me pika nga sekuenca 533 bp dhe vumë re se sekuenca përmbante përsëritje në miniaturë të përmbysur (Figura plotësuese 4b). Ne dërguam futjen 533 bp në BLAST kundrejt bazës së të dhënave MITE të impiantit, duke rezultuar në goditje të shumta nga familja MITE DTA_Sot42 në S. tuberosum15, duke treguar se futja 533 bp në promotorin e Rrëshqitje me të vërtetë e ka origjinën nga një TE (Fig. Suplementare 4c).
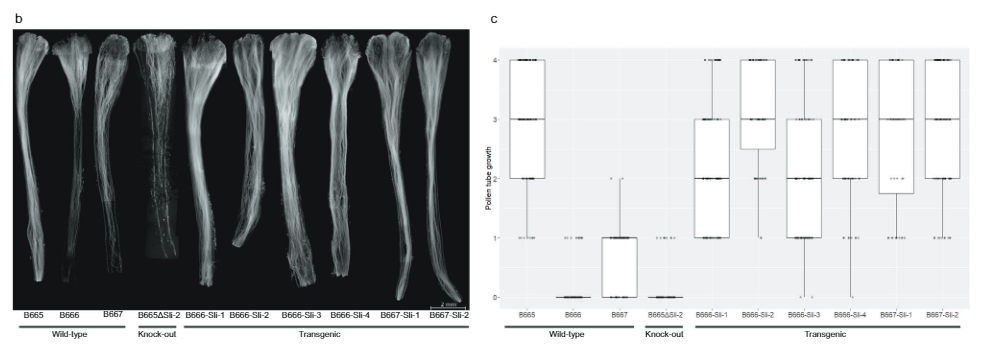
Për të konfirmuar më tej se PGSC0003DMG400016861 është me të vërtetë Rrëshqitje, ne projektuam një konstrukt shprehjeje që përmban ekzonet e alelit SC të Rrëshqitje ndërmjet promotorit dhe terminatorit të tij (Fig. 3a) në vektor pBINPLUS (pBINPLUS-Sli). Ne e përdorëm këtë konstrukt për të transformuar dy gjenotipe SI nga harta e popullsisë 18SC12. Ne fenotipuam dy deri në gjashtë klone nga secili prej pesë transgjenikëve të pavarur që rrjedhin nga gjenotipi SI B666 dhe tre transgjenikë që rrjedhin nga gjenotipi SI B667.
Klonet nga gjashtë transgjenikë të pavarur vendosin lehtësisht manaferrat pas vetëpjalmimit (Të dhënat Suplementare 3). Përveç kësaj, mikroskopi fluoreshent tregoi se poleni nga Rrëshqitje bimët transgjenike rriten më thellë në vetë-stile sesa kontrollet e patransformuara (Fig. 3b, c). Ne shënuam rritje të tubit të polenit në 442 vetëpllenime në Rrëshqitje transgjenikët dhe 179 vetëpjalmime në kontrolle të patransformuara në një shkallë 0-4. Shumica e tubave të polenit arrinin në vezoret në shumicën Rrëshqitje transgjenikët, krahasuar me vetëm një pjesë shumë të vogël të kontrolleve, duke treguar se PGSC0003DMG400016861 është Rrëshqitje gjen
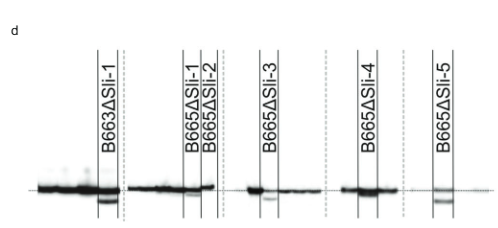
Më pas, ne projektuam një konstrukt CRISPR-Cas9 që kodon katër gARN që synojnë ekzonin e parë të PGSC0003DMG400016861 (pAGM:CRISPRASli, Fig. 3a). Ne transformuam dy gjenotipe SC (B665 & B663) me këtë konstrukt dhe morëm 149 rigjenerues të transformuar. Më pas analizuam ekzonin e synuar duke përdorur PAGE për të identifikuar INDEL-et e induktuara nga CRISPR-Cas9. Fatkeqësisht, vektori pAGM:CRISPRASli kishte një efikasitet të ulët, vetëm gjashtë nga 149 rigjeneruesit treguan INDEL në Rrëshqitje (Fik. 3d). Pesë nga këto linja CRISPR-Cas9 janë heterozigote për INDEL-et, por një linjë, B665ASli-2, është homozigote për një INDEL të vogël. Ndërsa B665 i patransformuar vendos lehtësisht manaferrat dhe tregon rritje të mirë të tubit të vetëpolenit përmes 105 stileve të vëzhguara, B665ASli-2 nuk vendos manaferrat pas vetëpjalmimit dhe poleni i tij nuk është në gjendje të rritet përmes 78 stileve të vëzhguara (Fig. 3b, c dhe të dhënat plotësuese 3), duke ofruar dëshmi të mëtejshme se PGSC0003DMG400016861 është me të vërtetë Rrëshqitje gjen
Në sistemet e vetë-papajtueshmërisë gametofitike të bazuara në S-RNase, vetë-fertilizimi parandalohet nga S-RNase të shprehura nga pistili që hyjnë në tubat e polenit dhe ushtrojnë efekte citotoksike në vetë-polen ose çdo polen tjetër që nuk ka një kuti S-Locus F të përputhshme (SLF ) proteina. Fekondimi i kryqëzuar mundësohet nga proteinat SLF të shprehura në polen që mund të njohin dhe detoksifikojnë S-RNase-të jo-vetë. Çdo S-alele kodon shumë SLF që secila prej të cilave mund të njohë një S-RNase të ndryshme dhe së bashku mund të njohin shumicën e S-RNase-ve të pranishme në patate, përveç S-RNase të koduar në të njëjtën S-alele. Sli kodon një proteinë F-box PP2-B10, e cila përbëhet nga një domen F-box i lidhur me një domen lektine. Dihet se domenet e lektinës ndërveprojnë me karbohidratet dhe mund të jenë në gjendje të ndërveprojnë me proteinat e glikoziluara16. Për më tepër, S-RNazat janë treguar të glikoziluara17. Ne supozojmë se futja 533 bp në promotorin e alelit SC të Sli mundëson shprehjen në polen, ku Sli është në gjendje të lidh dhe të detoksifikojë vetë S-RNases, duke çuar në humbjen e ndalimit të rritjes së tubit të vetë-polenit dhe rrjedhimisht vetë-përputhshmërisë. Një hetim i detajuar mbi aktivitetin e MITE në patate nga Laimbeer zbuloi se 2% e futjeve të MITE afër rajoneve gjenetike shoqëroheshin me ndryshime në shprehjen e gjeneve.
Për më tepër, nga 1935 futjet e testuara të hAT pranë rajoneve gjenetike, 13 rezultuan në rregullim të lartë të gjenit të lidhur, duke treguar se shprehja specifike e polenit e ndryshuar e Rrëshqitje mund të shkaktohet vërtet nga futja 533 bp në promotorin e saj18. Megjithatë, kërkohen kërkime të mëtejshme për të përcaktuar vlefshmërinë e kësaj hipoteze.
Më parë, Clot et al përdorën një qasje të ndarë në masë të hartës K-mer për të identifikuar një interval 333 kb në kromozomin 12 në të cilin duhet të vendoset Sli19. Këtu, ne hartuam vendndodhjen Sli në të njëjtin rajon të kromozomit 12 në një popullatë F1 dhe përdorëm një ekzaminim rekombinant për të reduktuar intervalin në 12.6 KB që përmban 2 gjene. Analiza e shprehjes zbuloi se aleli SC i njërit prej këtyre gjeneve shprehet në mënyrë specifike në polen nga gjenotipet SC. Së fundi, duke përdorur shprehjen transgjenike dhe eliminimin e shkaktuar nga CRISPR-Cas9, ne tregojmë përfundimisht se PGSC0003DMG400016861 është Sli. Ndërsa studimi nga Laimbeer tregoi se MITEs mund të rregullojnë gjenet e afërta në një mënyrë specifike të indeve, kërkohen më shumë kërkime për të provuar se prania e MITE në promotorin Sli është shkaku i shprehjes së tij specifike për polen.
Në materialet e hulumtuara në këtë studim (Të dhënat Suplementare 4), ne nuk mund të konfirmonim raportet e mëparshme të vdekshmërisë së lidhur me homozigozitetin për Sli, pasi gjetëm bimë të qëndrueshme F2 homozigote për Sli që ishin në gjendje të vendosnin manaferrat (Të dhënat Suplementare 1)12>20. Për më tepër, sekuencat e gjenomit të linjës inbred Solyntus, si dhe linjës inbred M6, tregojnë se të dyja këto linja janë homozigote për Sli, duke treguar se homozigoziteti për vetë Sli nuk është vdekjeprurës, megjithëse është ende e mundur që një vdekjeprurëse Aleli i lidhur gjenetikisht me Sli në një paraardhës është hequr nëpërmjet rikombinimit në këto gjenotipe21'22. Megjithatë, nga të dhënat e gjeneruara në këtë studim, nuk mund të përjashtojmë mundësinë që shtrembërimi i ndarjes i vërejtur në popullatën F2 të shkaktohet nga një alele vdekjeprurëse e lidhur në fazë me alelin SI të Sli. Deri më tani, është e paqartë nëse vetë Sli mund të njohë dhe detoksifikojë drejtpërdrejt S-RNases. Më tej, nuk është e qartë nëse Sli rezulton në vetëpërputhshmëri në të gjithë gjenotipet e S-lokusit. Është e mundur që funksioni i disa S-aleleve nuk mund të frenohet nga Sli. Nevojiten kërkime të mëtejshme për të zgjidhur këtë pyetje.
Ndërsa identifikimi i Sli-së mundëson më tej mbarështimin hibrid të bazuar në linjën inbred duke përdorur patate diploide, pengesa të tjera mbeten. Së pari, më e rëndësishmja, patatja diploide vuan nga depresioni i gjakderdhjes, gjë që çon në reduktimin e fuqisë dhe pjellorisë gjatë ngjizjes. Pastrimi i aleleve të dëmshme nëpërmjet vetëfertilizimit të vazhdueshëm të linjave diploide të patates është një metodë efikase për të reduktuar depresionin e brejtësve dhe tashmë ka rezultuar në gjenerimin e linjave të gjinisë së patates relativisht të fuqishme dhe pjellore.2'23-25. Së dyti, dhuruesi i Sli i përdorur në këtë studim, DS, rrjedh nga një S. kakoense aderimi, që mund të çojë në probleme me tërheqjen e lidhjes së aleleve të dëmshme nga S. kakoense. Në programin e mbarështimit diploid të Solyntës, ne nuk shohim probleme të dukshme për shkak të aleleve të dëmshme që vijnë nga S. chacoense. Për më tepër, një studim i kohëve të fundit mbi vetë-përputhshmërinë zbuloi se k-merët specifikë SC janë tashmë të pranishëm në disa kultivarë tetraploidë, duke ofruar një rrugë për të anashkaluar plotësisht këtë zvarritje të mundshme të lidhjes duke përdorur dihaploidët e krijuar nga këta kultivarë si donatorë Sli.19.
Metodat
Materialet bimore. Të gjitha materialet bimore të përdorura janë renditur në të dhënat plotësuese 4
Kushtet e serrës. Të gjitha bimët u rritën në serra që ngroheshin kur temperatura binte nën 14°C dhe ftoheshin duke hapur dritaret kur temperatura rritej mbi 19°C. Ndriçimi artificial plotësoi dritën natyrale kur intensiteti i dritës ra nën 85 W/M2. Bimët u rritën në një përzierje të veçantë të substratit të patates nga Lentse Potgrond (Lentse Potgrond BV, Katwijk, Holandë). Përzierja e substratit të përdorur përbëhet nga një përzierje torfe për marrjen e ekuilibruar të ujit, pleh bazë me çlirim të ngadaltë dhe gëlqere për të siguruar nivelin e kërkuar të pH. Përzierja e substratit u plehërua duke përdorur një zgjidhje 20:20:20 Azot: Fosfor: Kalium me një përçueshmëri elektrike (EC) prej 1.5.
Vlerësimi i vetë-përputhshmërisë. Lulet dhe sythat numëroheshin një herë në javë dhe fuqia shënohej një herë në muaj në një shkallë nga 1 në 9 ku 1 ishte një bimë jashtëzakonisht jo e fortë dhe 9 ishte një bimë jashtëzakonisht e fuqishme. Poleni nga lule të shumta nga një bimë u mblodh në një tub Eppendorf dhe u përdor menjëherë për vetëpllenim në të njëjtat lule me një maksimum prej 10 lulesh për bimë në javë. Bimët që vendosin më shumë se dy manaferra që përmbajnë të paktën 35 fara për vetë kokrra të kuqe u klasifikuan si vetë-përputhshme. Për të përcaktuar pjellorinë femërore, bimët u pjalmuan me polen të grumbulluar nga të paktën tre gjenotipe të palidhura. Bimët që nuk vendosën vetë-manaferrat pas të paktën 10 vetëpjalmimesh, por vendosën të paktën një kokrra të kuqe me shumicë dhe treguan polen pjellor në analizën mikroskopike të stileve të vetëpjalmuara, u klasifikuan si të papajtueshme. Për 40 gjenotipe nga popullatat e hartës në të cilat të dhënat e grupit të manaferrave dhe farave nuk ishin përfundimtare (17SC11: n = 14, 18SC11: n = 7, 18SC12: n = 19), klasifikimi fenotipik u bazua në rritjen e tubit të vetëpolenit përmes stileve (shënuar në të dhënat Suplementare 1).
Imazhi i stilit. Për të vizualizuar rritjen e tubit të polenit, stilet e pjalmuara u hoqën 24-48 orë pas pjalmimit dhe më pas u fiksuan në etanol: acid acetik 3:1 për të paktën 24 orë. Stilet më pas u maceruan në 8M NaOH për 10 minuta në 65 °C dhe u shpëla dy herë me ujë të dejonizuar. Stilet u vendosën në sllajde mikroskopike dhe u ngjyrosën për 2-5 minuta duke përdorur 0.1% aniline blu (Carl Roth GmbH) në 0.1 MK4P2O7 (pH = 7), më pas shtypet në glicerinë duke përdorur një mbulesë dhe vëzhgohet duke përdorur një mikroskop fluoreshent Zeiss Axiolab duke përdorur një grup filtri 01 (BP 365/12, FT 395 dhe LP 397). Të gjitha stilet u vëzhguan dhe u vlerësuan duke përdorur dy parametra: (1) depërtimi më i thellë në stil, siç shprehet në përqindjen e depërtimit maksimal, (2) % e tubave të polenit që arrijnë penetrimin më të thellë. Më pas ne i konvertuam këto përqindje në një shkallë 0-4, ku stilet në të cilat asnjë tub poleni nuk arrinte vezoren morën një rezultat 0, stilet në të cilat midis 0 dhe 25% e tubave të polenit morën rezultatin 1, stilet në të cilat midis 25 dhe 50% e tubave të polenit arritën në vezoren morën rezultatin 2, stilet në të cilat midis 50 dhe 75% e tubave të polenit arritën në vezoren morën rezultatin 3 dhe stilet në të cilat më shumë se 75% e tubave të polenit arritën në vezoren morën një rezultat prej 4.
Përvetësimi i imazhit. Stilet e zgjedhura u fotografuan duke përdorur një mikroskop Zeiss Axiophot me grup filtri 01, duke përdorur një Zeiss AxioCam ICc 5. Imazhet u bënë duke përdorur paketën softuerike Zeiss Zen 2.3 (edicion blu). Gjatë blerjes, cilësimet u rregulluan për të minimizuar sfondin. Stilet u fotografuan duke përdorur objektivin x5 dhe u ruajtën si skedarë TIFF me një rezolucion prej 2464 x 2056 piksele me thellësi 24-bit. Deri në tetë imazhe të veçanta u mblodhën më pas duke përdorur montuesin e imazheve Panavue. Kontrasti dhe shkëlqimi i stileve të mbledhura u rregulluan për të krijuar Fig. 1a dhe 3c.
Ekstraktimi i ADN-së. Për analizën KASP të popullatave të hartës, mostrat e gjetheve u dërguan në VHLGenetics (Wageningen, Holandë) për nxjerrjen e ADN-së duke përdorur kits sbeadex™ (LGC Genomics GmbH, Berlin, Gjermani) sipas protokollit të dhënë nga prodhuesi.
Analiza e KASP. Analiza kompetitive e PCR (KASP™) specifike e alelit u krye nga VHLGenetics (Wageningen, Holandë) duke përdorur analizat KASP të dizajnuara për të qenë specifike për SNP-të që ndahen në materialin tonë. Analizat e KASP u kryen sipas protokollit të ofruar nga prodhuesi (LGC Genomics GmbH, Berlin, Gjermani). Rezultatet nga analizat KASP u vizualizuan duke përdorur SNPviewer (i disponueshëm në lgcgroup.com/products/genotyping-software/snpviewer) për të konfirmuar ndarjen e saktë dhe thirrjen e gjenotipit.
Analiza e lidhjes. Haplotipet e prindërve femra të vetë-përputhshme u rindërtuan nga të dhënat e gjenotipit duke analizuar shkallët e rikombinimit midis SNP-ve të ndryshme. Këto të dhëna u përdorën për të kthyer thirrjet SNP në një format "axb", ku haplotipi "a" është i lidhur me alelin e vetëpërputhshëm të Sli, ndërsa haplotipi "b" është i lidhur me një alel të vetë-papajtueshëm të Sli. Hartat e lidhjeve u krijuan duke përdorur Joinmap 4.126 me llojin e popullsisë DH dhe cilësimet e paracaktuara.
Harta QTL. Të dhënat e fenotipit u konvertuan në një tipar numerik duke caktuar 1 për secilin gjenotip të vetë-përputhshëm, 0 për secilin gjenotip të vetë-papajtueshëm dhe * për gjenotipet për të cilat përputhshmëria nuk mund të përcaktohet. Hartëzimi i QTL u krye duke përdorur hartën e intervalit në MapQTL27. Rezultatet e MapQTL u përdorën për të gjeneruar parcela QTL me Mapchart 2.328.
Analiza bioinformatike. Për të identifikuar modelet e sakta të gjeneve në intervalin fillestar prej 27.37 kb, ne hetuam dy shënime të gjeneve të veçanta për gjenomin e referencës DM4.04, shënimin PGSC dhe shënimin ITAG. Shih gjithashtu Hirsch et al.29. Për të konfirmuar korrektësinë e shënimeve, ne kryem kërkime BLASTp me sekuencat e parashikuara të proteinave nga të dy shënimet. Duke krahasuar rezultatet më të mira në kërkimin BLASTp me pyetjen tonë, ne përcaktuam nëse të gjitha ekzonet dhe domenet e shënuara në sekuencën e parashikuar të proteinave mbështeteshin nga proteina të ngjashme në patate dhe specie të tjera bimore. Për më tepër, bibliotekat e ARN-seq të disponueshme publikisht në SPUD DB (e disponueshme në solanaceae.plantbiology.msu.edu/cgi-bin/ gbrowse/potato/) dhe shikuesin e të dhënave të gjenomit NCBI (e disponueshme në ncbi.nlm.nih.gov/ genome/gdv /browser/) u përdorën për të përcaktuar nëse ekzonet e supozuar kishin prova shprehëse. Së bashku, këto dy qasje na lejuan të vërtetojmë strukturat intron-ekson të modeleve të gjeneve në të dy shënimet, duke rezultuar në një zgjedhje të informuar për një ose më shumë izoforma të modeleve të gjeneve për të përfaqësuar gjenin në fjalë. Bazuar në këto qasje, gjeni i kandidatit PGSC0003DMG400016862 u njoh si i pjesshëm dhe i shprehur në mënyrë të parëndësishme dhe u hodh poshtë nga analizat e mëtejshme. Modeli i gjenit Sotub12g029970 u konsiderua i saktë, ndërsa homologu i tij PGSC PGSC0003DMG400016860 ka të ngjarë të jetë i cunguar. Për shkak se ndodhet kryesisht jashtë intervalit të caktuar dhe nuk mund të identifikohej asnjë zëvendësim përkatës i aminoacideve midis bimëve SC dhe SI, ky gjen u hoq nga analizat e mëtejshme.
Analiza e variacionit. Për të identifikuar mutacionet në intervalin 27.37 kb që janë specifike për gjenotipet e vetëpërputhshme, të gjitha SNP-të me besim të lartë (Të dhënat Suplementare 3) u përcaktuan që ishin (1) homozigotë në DS, 17SC100-18 dhe 17SC100-2 (sepse të tre janë homozigotë për aleli SC i Sli (Sli/Sli')'), (2) homozigot i ndryshëm në D16 (sepse D16 është homozigotë për alelin SI të Sli (sli/sli)), dhe (3) heterozigotë në të dy 16HP1-66 dhe 17SC25-8 (sepse të dy janë heterozigotë për alelin SC Sli (Sli /sli)). Sekuenca alelike u mor nga montimi de novo duke përdorur versionin 3.11.1 SPAdes30 prej 150 nt të dhëna Illumina me fund të çiftuar të impianteve të listuara më sipër (me një thellësi renditjeje afërsisht 25-30X). Kontigat që rezultuan u rreshtuan me referencën DM (duke përdorur versionin 2 të minimap2.1) dhe u filtruan për ato që rreshtoheshin në mënyrë të besueshme në 27 kb. Nga këto lidhje të rreshtuara, variacioni në lidhje me DM4.03 u përcaktua në sasi të drejtpërdrejtë (duke përdorur nënprogramet mpileup dhe thirrje nga bcftools, versioni 1.9) dhe u rendit në Formatin e Thirrjes Variant (VCF).
Analiza e ndryshimit të aminoacideve. Nga kjo listë e mutacioneve specifike të SC, të gjitha SNP-të jo-sinonimike u identifikuan duke mbivendosur me ekzonët e caktuar kodues. Ndryshimet e aminoacideve në lidhje me sekuencën DM ose SI janë renditur. Ndryshimet unike të aminoacideve u identifikuan duke kryer kërkime BLASTp duke përdorur sekuencën e proteinave dhe duke kryer rreshtim të shumëfishtë të sekuencave duke përdorur 100 goditjet më të mira të BLASTp.
Ndryshimet në rajonet e promotorit dhe të terminatorit. Rajoni promotor u zgjodh të jetë sekuenca në rrjedhën e sipërme të kodonit fillestar deri në sekuencën koduese të gjenit në rrjedhën e sipërme me një maksimum prej 1500 nt. Ndryshime dramatike në rajonet promotore u gjetën brenda intervalit 27.37 kb, nga të cilat më të habitshmet ishin disa fshirje më të mëdha dhe futje të dhjetëra deri në qindra nukleotideve të gjatësisë. U morën të gjitha ndryshimet në intervalin Sli, në lidhje me DM, duke përfshirë atë të rajonit të promotorit/në rrjedhën e sipërme si dhe të rajonit të terminatorit/në rrjedhën e poshtme.
Marrja dhe mbirja e polenit. Poleni nga gjenotipet e listuara në Fig. 2a është marrë duke vibruar lule të hapura duke përdorur një furçë dhëmbësh elektronike dhe duke mbledhur polenin në tuba Eppendorf 1.5 ml. Pas marrjes, poleni u tha duke ruajtur tubat e hapur Eppendorf me polen në një kuti të mbyllur me ajër që përmban xhel silicë për 24 orë në temperaturën e dhomës. Më pas, poleni u ruajt në -20 °C deri në përdorim të mëtejshëm.
Poleni mbinte duke pezulluar 2.5 mg polen të tharë në 5 ml medium të lëngshëm (9% (w/v) saharozë, 50 mg/l acid borik, 73.5 mg/l CaCly2H2O, 118 mg/l Ca (NO3) 24H2O, 123 mg/l MgSO.4VH2O) në enë Petri me diametër 3.5 cm të mbyllura me parafilm. Poleni u la të mbijë në enët Petri për 24 orë në errësirë në një inkubator tundës në temperaturën e dhomës dhe duke u tundur në 125 RPM. Mjeti i lëngshëm që përmban polenin e mbirë u fut me kujdes në tuba Eppendorf 2 ml duke përdorur majat e pipetës që u modifikuan për të rritur madhësinë e hapjes në mënyrë që të mos dëmtojnë tubat e polenit. Tubat Eppendorf më pas u centrifuguan në 600xg për 1 min dhe mjedisi u hoq me kujdes me anë të pipetimit. Peleti dhe disa mediume të mbetura u ngrinë menjëherë në azot të lëngshëm, u shtuan dy rruaza çeliku inox (diametër 2 mm) dhe mostrat u bluan duke përdorur një TissueLyser II (Qiagen GmbH, Hilden, Gjermani) në 20 Hz për 1 min.
Ekstraktimi dhe sekuenca e ARN-së. Buffer RLT (Qiagen GmbH) iu shtua kampioneve të polenit të grirë duke u siguruar që mostrat të mbetën të ngrira. Ekstraktimi i ARN-së u krye më pas duke përdorur mini kitin RNeasy sipas protokollit të prodhuesit (Qiagen GmbH, Hilden, Gjermani). Bibliotekat cDNA të madhësisë së insertit 250-300 bp u renditën si lexime të çiftëzuara 150 nt, duke dhënë 30-42 milionë çifte leximi për mostër (Novogene, Kembrixh, Mbretëria e Bashkuar).
Komplete të tjera të të dhënave ARN-seq. Për të krijuar një përmbledhje të niveleve të shprehjes (specifike për indet), të gjitha grupet e të dhënave të sekuencës së ARN-seq me fund të çiftëzuar të etiketuar si ORGANISM "Sola-num tuberosum" u shkarkuan nga domeni publik (NCBI-SRA, datë 2018/17/13), në total 441 grupe të dhënash të çiftuara fastq. Nga këto 441 grupe të dhënash publike, 3 u krijuan nga indet e stilit (SRR7402817-SRR7402819) dhe të gjithë të tjerët nga inde të ndryshme jo-polen, fazat e zhvillimit dhe ngjitjet e bimëve.
Asambleja e referencës Solyntus. Për analizat e shprehjes, drafti i fituar së fundi i linjës së referencës homozigote Solyntus (versioni 1.0, i shkarkueshëm në www.plantbreeding.wur.nl/Solyntus/) është përdorur si gjenom referues. Solyntus është një varietet në thelb homozigot i krijuar si pjesë e programit të mbarështimit të Solynta21. Intervalet e hartës në këtë studim u konkluduan nga asambleja e gjenomit DM v4.0331 në asamblenë e gjenomit Solyntus 1.0 nga kërkimet bazë të ngjashmërisë (duke përdorur BLASTn dhe veglat e shtratit) për t'u vendosur në (koordinatat e montimit të gjenomit Solyntus 1.0) 53532708-53954293 (Intervali I, 421.6 kb < —628.9-53683239, 53867377 , 184.1 , 168.7 . kb< — 53731620kb), 53763003-31.4 (Intervali III, 27.4kb< —53753977kb) dhe 53763003-9.0 (Intervali IV, 12.6kb < —1.0 kb), respektivisht. Midis kllapave janë numri i intervalit të njëpasnjëshëm të hartës [Koordinatat Solyntus 1.0], madhësia në Solyntus-4.03 dhe madhësia në DM-4.04/4.03, respektivisht. Të gjitha intervalet janë të vendosura në kromozomin ST12ch12_RaGOO (duke qenë kromozomi 1.0) dhe nuk përmbajnë asnjë boshllëk të vetëm në montimin Solyntus 4.03. Variacioni i madhësisë së intervalit shkaktohet nga një mori boshllëqesh (N) në sekuencën përkatëse DM dhe variacion të gjerë midis të dy gjenomave. Intervalet përkatëse në gjenomën e DM (DM-4.04/12): Intervali I: chr58601503:59230363-12, Intervali II: chr58962004:59130723-59016142; Intervali III: 59043512-12; Intervali IV: chr59030880:59043512-XNUMX.
Shënimi i gjeneve në Solyntus 1.0 u konkludua nga tre katalogë të ndryshëm gjenesh (patate DM4.03, ITAG4.0 Publikimi i shënimit të gjenomit të domates më 6 shtator 201932, dhe Pepper-v. 1.5533), të cilat u hartuan në asamblenë Solytus duke përdorur GeMoMa (v1.6.1). Kjo është bërë për të kompensuar papërsosmëritë në katalogët individualë të gjeneve dhe për të maksimizuar ndërgjegjësimin tonë për ekzistencën e gjeneve të mundshme dhe/ose lokacioneve të shprehura.
Kuanti i bollëkut të leximit dhe transkriptimit të ARN-seqfidosja. Të gjitha 5 SC, 3 SI dhe të gjitha 441 grupet e të dhënave publike të ARN-seq u hartuan në gjenomin e referencës Solyntus duke përdorur hisat2 (versioni 2.1.0). Katalogu i gjeneve hibride i marrë duke përdorur GeMoMa u përdor për vlerësimin e bollëkut të drejtuar nga transkripti duke përdorur StringTie (versioni 2.1.1) me cilësimet -t -c 5 -f 0.05 -G dhe një skedar Solyntus1.0 gff të lidhur me GeMoMa. Të gjitha shprehjet e vëzhguara në një interval prej 500 kb që rrethon Rrëshqitje u vlerësua lokusi si qendër, në të cilin interval ndodhen gjithsej 90 lokuse gjene (të konkluduara). Ne konfirmuam mungesën e ndonjë shprehjeje të dukshme në mostrat SC jashtë ndonjë prej këtyre lokacioneve gjenike. Në intervalin 500 kb, ne treguam më pas numrin më të vogël të gjeneve kandidate kur kryqëzohen me intervalet tona të hartës I-IV siç përcaktohen më sipër.
mefirmacioni i haplotip-specific shprehje. Nga 90 lokacione të shprehura në intervalin 500 kb, vetëm 8 u shprehën mbi një prag të zgjedhur prej 20 FPKM në të gjitha mostrat SC/SI. Ne i përdorëm këto vende për të matur dallimet në nivelet e shprehjes specifike të haplotipit (Sli ose sli). Pragu i shprehjes i zgjedhur mundësoi një thellësi të mjaftueshme të leximit për ta ndarë përfundimisht dhe në mënyrë të besueshme shprehjen në (maksimumi) 2 haplotipe. Së bashku me vetë vendndodhjen PSC (të cilit i mungon shprehja në bimët SI), këto 8 + 1 lokacione u haplotipizuan në secilin prej 8 mostrave (versioni i fazës SAMtools 1.7, cilësimet e paracaktuara). Skedarët fastq të haplotipizuar (të çiftuar) që rezultuan u mblodhën de novo duke përdorur SPAdes (versioni 3.11.1). Kontigat që rezultuan u filtruan për bollëk të bollshëm dhe mRNA të supozuara me gjatësi të plotë, që korrespondojnë me izoformën kryesore (haplotipike) të shprehur. Në disa raste, kjo hoqi izoformat e bashkuara në mënyrë alternative, asnjëra prej të cilave nuk u mbështet nga lexime të bollshme për të pasur ndonjë rëndësi të dukshme biologjike. Variacioni në këto sekuenca të mARN-së të haplotipizuar u përdor për të (mos)konfirmuar nëse një ose të dy haplotipet shpreheshin në secilin nga lokuset/kampionët përkatës.
Dizajni i Rrëshqitje konstrukt shprehjesh. Ne përdorëm sekuencën e bimës dhuruese Sli DS për të dizajnuar kasetën e shprehjes Sli. Për të lejuar shprehjen amtare të PSC, ne ndërtuam një sekuencë të acidit nukleik që përfshin promotorin vendas (1563 bp në rrjedhën e sipërme të kodonit fillestar), tre ekzonet dhe terminatorin vendas (740 bp në rrjedhën e poshtme të kodonit ndalues). Kështu, të dy intronet u hoqën nga PSC gjen i bimës dhuruese DS. Kjo sekuencë u sintetizua dhe u klonua në pBINPLUS nga Genscript (Genscript Biotech, Leiden, Holandë). Ne i referohemi vektorit që përmban Rrëshqitje futet si pBINPLUS-Sli.
Ndërtimi i CRISPR-vektor Cas9. Ne projektuam katër gARN bazuar në sekuencën e PGSC0003DMG400016861 në DM4.03 në vende ku nuk kishte asnjë ndryshim midis aleleve SC dhe SI. Për zgjedhjen e udhëzuesve të përshtatshëm dhe ndërtimin e vektorit, ne përdorëm metodën e përshkruar nga Santillan Martinez et al.34. Shkurtimisht, katër sgARN u zgjodhën sipas udhëzimeve të përshkruara nga Liang et al.35. Mjeti i parashikimit të objektivit CC-Top CRISPR/Cas9 u përdor për të gjeneruar një listë të sgARN-ve36, palosja u vlerësua duke përdorur ueb serverin Mfold37, dhe aktiviteti i sgARN-ve u parashikua duke përdorur shënuesin e sgRNA38. Udhëzuesit e mëposhtëm u zgjodhën dhe u përdorën për të ndërtuar vektorin pAGM:CRISPRASli: ekzon5.1T01 (ATTTTCATCCGCGATCTCTCGGGG), ekzon5.1T04 (GATTTCA TCCGCGATCTCTCGGG), ekzon5.1T06 (TATTTCCTATTGCTACACAGATCGTCGT, exon5.1. Më pas, konstrukti CRISPR u sintetizua duke përdorur plazmide të marra nga Addgene: pICH07 (shabllon për amplifikimin); pICSL86966 (plazmidi i nivelit 01009); pICH0, pICH47751, pICH47761, pICH47772 dhe pICH47781 (plazmidet e nivelit 47732); pICH1 (lidhës për katër udhërrëfyes); dhe pAGM41822 (vektor binar i nivelit 4723). Plazmidi u klonua duke përdorur E. coli DH5a dhe plazmidi i pastruar u dërgua për renditje duke përdorur primerët PDS5843 (TTTGTGATGATGCTCGTCAGGGGG), PDS8535 (CCCGAGAATTATGCAGCATT TT) PDS8536 (TCATCAGTAATTACGGGGGCT) dhe AL717GTAATTACGGGGGCT (TCATCAGTAATTACGGGGGCT) dhe AL9GTGATGATGGGGGCT, dhe ALXNUMXGTGATGATGATGGGGCT, dhe ALXNUMXCCATGAT të gjitha komponentët, dhe orientimi i ALXNUMXCCATGCT
Transformimi i pBINPLUS-Sli dhe pAGMzCRISPRASli vektor në Agrobacterium tumefaciens. Ne e transformuam pBINPLUS-Sli në A. tumefaciens tendosni AGL0 dhe pAGM:CRISPRASli në A. tumefaciens shtamet AGL0 dhe AGL1 duke përdorur një protokoll elektroporimi. Morëm 40 pl qeliza kompetente AGL0 dhe shtuam 110 pl ujë milliQ të ftohtë në akull. Vendosëm 50 pl të kësaj përzierjeje në tuba Eppendorf të ftohur paraprakisht në akull dhe shtuam 1 pl plazmid. Ne i lamë qelizat në akull për 15 minuta dhe i transferuam qelizat në kuvetat e elektroporimit të ftohura paraprakisht. Ne i elektroporosëm përzierjet me një Micropulser™ (Bio-Rad Laboratories, Vee-nendaal, Holandë) duke përdorur programin Ec1 (1.8 kV, kuvetë 0.1 cm). Shtuam 1 ml LB dhe i inkubuam qelizat për 3 orë në një shaker në 28 °C dhe 200 RPM. Më pas, ne inokuluam pllaka agar LB që përmbajnë Rifampicin (100 pg/ml) dhe Kanamycin (50 pg/ml) me kulturën e transformimit. Të gjitha kolonitë e zgjedhura u konfirmuan se përmbajnë vektorin e saktë.
Transformimi i gjenotipeve të patates. Ne i transformuam gjenotipet B666 dhe B667 me pBINPLUS-Sli dhe gjenotipet B663 dhe B665 me vektorin pAGM:CRISPRASli duke përdorur metodën e eksplantit të kërcellit të përshkruar nga Visser39. Shkurtimisht, eksplantet internode u morën nga gjenotipe të rritur in vitro dhe u vendosën në enët Petri që përmbajnë mjedis R3B me 2 ml medium PACM. Të nesërmen, 50 ml 48 h Agrobakter kulturat u centrifuguan dhe u risuspenduan në 75 ml LB. Eksplantet internode më pas u zhytën në Agrobakter suspension për 5 min, thahet në filtër dhe vendoset përsëri në enët Petri që përmbajnë medium R3B. Pas 48 orësh inkubimi, eksplantet u transferuan në enët Petri që përmbajnë MS20 me antibiotikë dhe u vendosën në një dhomë rritjeje për të lejuar rigjenerimin e lastarëve. Pas rigjenerimit, lastarët u rritën në një mjedis MS20 që përmban cefotaksime (200 pg/ml), vankomicinë (200 pg/ml) dhe kanamicinë (100 pg/ml). Kur lastarët arritën gjatësinë e mjaftueshme, u bënë prerje dhe u rritën në MS20 pa antibiotikë. Pas të paktën dy javësh rritje në MS20 pa antibiotikë, bimët u mbollën në serë.
Analiza e ploidisë. Ploidia e bimëve transgjenike si dhe kontrollet e patransformuara u përcaktuan duke përdorur citometrinë e rrjedhës nga Shërbimet e Citometrisë së Bimëve (Didam, Holandë). Të gjithë rigjeneruesit tetraploidë u hodhën poshtë.
Analiza FAQE e CRISPR-Mutacionet e shkaktuara nga Cas9. Ekstraktimi i ADN-së, PCR dhe analiza PAGE u krye nga Limgroup (Horst, Holandë). Primerët e mëposhtëm u përdorën për të përforcuar rajonin e synuar CRISPR-Cas9: Primer përpara: CTATTTCCTATTGCTACCAG, primer i kundërt: AAACTTTACCCAAAT AACGTC. Etiketimi i produkteve PCR u arrit duke shtuar një primer të kundërt me një bisht M13 (sekuenca e primerit: TGTAAAACGACGGCCAGTAAACTTTAC CCAAATAACGTC) dhe ose 700 IRDye ose 800 IRDye të etiketuar M13 në përzierjen PCR. Produktet PCR që rezultuan u analizuan në PAGE duke përdorur një sistem Li-cor. Produktet PCR nga shumica e linjave pa mutacione të induktuara nga CRISPR-Cas9 u ndanë nga imazhet e xhelit për të prodhuar Fig. 3d (ekcizionet e treguara me vija të ndërprera).
Analiza filogjenetike e futjes 533 bp. Sekuenca e futjes 533 bp u analizua duke përdorur BLASTn në faqen e internetit të NCBI. 30 hitet më të mira, duke përfshirë futjen e pranishme në Rrëshqitje në Solyntus, më pas u shkarkuan dhe u rreshtuan në MegAlign Pro 17 (DNASTAR) duke përdorur MUSCLE me cilësimet e paracaktuara. Pemët u krijuan duke përdorur algoritmin e bashkimit fqinj me cilësimet e paracaktuara.
Raportimi përmbledhës. Informacione të mëtejshme mbi hartimin e kërkimit janë në dispozicion në Përmbledhjen e Raportimit të Kërkimit të Natyrës lidhur me këtë artikull.
Disponueshmëria e të dhënave
Sekuenca e gjenomit Solyntus dhe leximet e sekuencave të papërpunuara janë të disponueshme në NCBI nën hyrje PRJNA631911. Asambleja dhe skedarët e shënimeve të gjenomit Solyntus janë në dispozicion nga WUR [https://www.plantbreeding.wur.nl/Solyntus/]. Të dhënat e sekuencës së ARN-së nga poleni i mbirë janë të disponueshme në arkivin e leximit të shkurtër të NCBI nën hyrje PRJNA713577. Të dhëna të tjera janë të disponueshme në skedarin e të dhënave burimore ose do të vihen në dispozicion sipas kërkesës. Të dhënat burimore janë dhënë me këtë punim.
Marrë: 22 janar 2021; Pranuar: 8 qershor 2021;
Botuar në internet: 06 Korrik 2021
Referencat
- 1. Duvick, DN Kontributi i mbarështimit për të dhënë përparime në misër (Zea provime maji L.). Adv. Agron. 86, 83-145 (2005).
- 2. Lindhout, P. et al. Drejt mbarështimit hibrid të farës së patates F1. Patate Res. 54, 301-312 (2011).
- 3. Jansky, SH et al. Rishpikja e patates si një kulture diploide e bazuar në linja inbred. Crop Sci. 56, 1412-1422 (2016).
- 4. Ye, M. et al. Gjenerimi i patateve diploide të vetë-përputhshme me nokaut të S-RNase. Nat. Bimët 4, 651-654 (2018).
- 5. Enciso-Rodriguez, F. et al. Tejkalimi i vetë-papajtueshmërisë në patatet diploide duke përdorur CRISPR-cas9. Fronti. Shkencat e bimëve. 10, 1-12 (2019).
- 6. Su, Y. et al. Introgresioni i gjeneve për rezistencë ndaj Fytophthora infektuese në patate diploide. Jam. J. Potato Res. 97, 33-42 (2020).
- 7. Dzidzienyo, DK, Bryan, GJ, Wilde, G. & Robbins, TP Diversiteti alelik i aleleve S-RNase në speciet diploide të patates. Teor. Aplikim Genet. 129, 1985-2001 (2016).
- 8. McClure, B., Cruz-Garcia, F. & Romero, C. Përputhshmëria dhe papajtueshmëria në sistemet e bazuara në S-RNase. Ann. Bot. 108, 647-658 (2011).
- 9. Kubo, K. et al. Sistemi bashkëpunues i jo-njohjes së vetvetes në vetë-papajtueshmërinë e bazuar në S-RNase. Shkencë 330, 796-799 (2010).
- 10. De Jong, H. & Rowe, PR Inbreeding në patatet diploide të kultivuara. Patate Res. 14, 74-83 (1971).
- 11. Hermsen, JGT & Olsder, J. Gjenetika e vetë-përputhshmërisë në dihaploidet e Patate L. 1. Sjellja e mbarështimit të dy dihaploidëve të vetëpërputhshëm. Eufytica 25, 597-607 (1976).
- 12. Hosaka, K. & Hanneman, RE Jr. Gjenetika e vetë-përputhshmërisë në një specie patate të egër diploide të vetë-papajtueshme Solanum chacoense. 1. Zbulimi i një gjeni të inhibitorit të lokusit S (Sli). Eufytica 99, 191-197 (1998).
- 13. Hosaka, K. & Hanneman, RE Jr. Gjenetika e vetë-përputhshmërisë në një specie patate të egër diploide të vetë-papajtueshme Solanum chacoense. 2. Lokalizimi i një gjeni të inhibitorit të Slikut (Sli) në gjenomën e patates duke përdorur shënuesit e ADN-së. Eufytica 103, 265-271 (1998).
- 14. Birhman, RK & Hosaka, K. Prodhimi i pasardhësve inbred të patateve diploide duke përdorur një gjen frenues S-locus (Sli) dhe karakterizimi i tyre. Genome 502, 495-502 (2000).
- 15. Chen, J., Hu, Q., Zhang, Y., Lu, C. & Kuang, H. P-MITE: një bazë të dhënash për elementët e transpozueshëm me miniaturë të përmbysur-përsëritës të bimëve. Acidet nukleike Res. 42, 1176-1181 (2014).
- 16. Stefanowicz, K., Lannoo, N. & Van Damme, EJM Plant F-box proteins — gjykon mes jetës dhe vdekjes. Crit. Rev. Plant Sci. 34, 523-552 (2015).
- 17. Liu, B., Morse, D. & Cappadocia, M. Glikozilimi i S-RNases mund të ndikojë në pragjet e refuzimit të polenit në Solanum chacoense. J. Exp. Bot. 59, 545-552 (2008).
- 18. Laimbeer, FPE Gjenomika e patates në tre mënyra: përcaktimi sasior i endoreduplikimit në zhardhokët, një rrëshqitje nëpër terrenin e transpozonit dhe sqarimi i rregullimit të ngjyrës së luleve. http://hdl.handle.net/10919/84480 (2018).
- 19. Clot, CR et al. Origjina dhe shfaqja e përhapur e vetëpërputhshmërisë me bazë Sli në patate. Teor. Aplikim Genet. https://doi.org/10.1007/s00122-020-03627-8 (2020).
- 20. Endelman, J., Jansky, SH, Butler, N. & Christensen, G. Dëshmi gjenetike e një alele vdekjeprurëse recesive në kromozomin e patates raporti 12-vjetor i Shoqatës së Patates së Amerikës. Jam. J. Potato Res. 96, 331 (2019).
- 21. van Lieshout, N. et al. Solyntus, gjenomi i ri i referencës shumë i afërt për patatet (Solanum tuberosum). G3 Genet Gjenomet Genet. 10, 3489-3495 (2020).
- 22. Leisner, CP et al. Sekuenca gjenomike e M6, një klon i lindur diploid i specieve të patates me zhardhok që prodhon shumë glikoalkaloid Solanum chacoense, zbulon heterozigozitetin e mbetur. Bima J. 1967, 562-570 (2018).
- 23. Peterson, BA et al. Vetë-fertiliteti në një popullatë patate diploide të kultivuar të ekzaminuar me grupin e polimorfizmit me një nukleotid të patates infinium 8303. Gjenomi i bimëve https://doi.org/10.3835/plantgenome2016.01.0003 (2016).
- 24. Lian, Q. et al. Përvetësimi i mutacioneve të dëmshme gjatë poliploidizimit të patates. J. Integr. Biol Biol. 61, 7-11 (2019).
- 25. van Lieshout, N. et al. Solyntus, gjenomi i ri i referencës shumë i afërt për patatet (Solanum tuberosum). G3 Genet Gjenomet Genet. 631911, g3.401550.2020 (2020).
- 26. Van Ooijen, JW JoinMap®4, Softuer për Llogaritjen e Hartave të Lidhjeve Gjenetike në Popullatat Eksperimentale Vëll. 33 (Kyazma BV, 2006).
- 27. van Ooijen, JW Saktësia e përcaktimit të vendndodhjeve sasiore të tipareve në speciet autogame. Teor. Appl Genet. 84, 803-811 (1992).
- 28. Voorrips, RE Mapchart: softuer për paraqitjen grafike të hartave të lidhjeve dhe QTL-ve. J. Hered. 93, 77-78 (2002).
- 29. Hirsch, CD et al. Spud DB: një burim për sekuencat e minierave, gjenotipet dhe fenotipet për të përshpejtuar mbarështimin e patates. Gjenomi i bimëve. 7, https://doi.org/ 10.3835/gjenomi bimor2013.12.0042 (2014).
- 30. Bankevich, A. et al. SPAdes: një algoritëm i ri i montimit të gjenomit dhe aplikimet e tij në sekuencën me një qelizë të vetme. J. Comput. Biol. 19, 455-477 (2012).
- 31. Sharma, SK et al. Ndërtimi i pseudomolekulave referente në shkallë kromozomi për patatet: integrimi i gjenomit të patates me hartat gjenetike dhe fizike. G3 Genet Gjenomet Genet. 3, 2031-2047 (2013).
- 32. Fernandez-Pozo, N. et al. Rrjeti i Gjenomikës Sol (SGN) - nga gjenotipi në fenotip tek shumimi. Acidet nukleike Res. 43, D1036-D1041 (2015).
- 33. Kim, S. et al. Sekuenca gjenomike e specit djegës ofron njohuri mbi evolucionin e pikasisë në pjepër specie. Nat. Genet. 46, 270-278 (2014).
- 34. Santillan Martinez, MI et al. Mutagjeneza e synuar nga CRISPR/Cas9 e gjenit të ndjeshmërisë së domates PMR4 për rezistencë ndaj mykut pluhur. BMC Plant Biol. 20, 1-13 (2020).
- 35. Liang, G., Zhang, H., Lou, D. & Yu, D. Përzgjedhja e sgARN-ve shumë efikase për redaktimin e gjenomit të bimëve me bazë CRISPR/Cas9. Sci. Reps. 6, 1-8 (2016).
- 36. Stemmer, M., Thumberger, T., Del Sol Keyer, M., Wittbrodt, J. & Mateo, JL CCTop: një mjet intuitiv, fleksibël dhe i besueshëm për parashikimin e objektivave CRISPR/Cas9. PLoS ONE 10,1-11 (2015).
- 37. Zuker, M. Mfold web server për palosjen e acidit nukleik dhe parashikimin e hibridizimit. Acidet nukleike Res. 31, 3406-3415 (2003).
- 38. Chari, R., Yeo, NC, Chavez, A. & Church, GM SgRNA Scorer 2.0: një model i pavarur nga speciet për të parashikuar aktivitetin CRISPR/Cas9. ACS Synth. Biol. 6, 902-904 (2017).
- 39. Visser, RGF in Manuali i Kulturës së Indeve Bimore 301-309 (Springer, 1991).
Interesat konkurruese
Autorët nuk deklarojnë interesa konkurruese.
Informacion shtesë
Informacione plotësuese Versioni online përmban materiale shtesë të disponueshme në https://doi.org/10.1038/s41467-021-24267-6.
korrespondencë dhe kërkesat për materiale duhet t'i drejtohen CWBB
Informacion për vlerësimin e kolegëve Nature Communications faleminderit Roger Chetelat dhe recensentët e tjerë anonimë për kontributin e tyre në rishikimin e kësaj pune. Raportet e rishikimit të kolegëve janë në dispozicion.
Ribotimet dhe informacionet e lejeve është në dispozicion në http://www.nature.com/reprints
Botues's shënim Springer Nature mbetet neutrale në lidhje me pretendimet e juridiksionit në hartat e publikuara dhe përkatësitë institucionale.
Mirënjohje
Ne e pranojmë ndihmën e Veronica Tammy Soputro në transformimin e dy gjenotipeve të patates me pAGM:CRISPRASli, ndihmën e studentëve BSc dhe MSc Gilo Pleunis, Iris Smits, Niki Vorgia, Hidde Knuiman, Maurice Geurts, Anja van Heteren, dhe Torsten van Heteren, Schriek për ndihmën e tyre në fenotipizimin e popullatave të hartës, dhe Tess Lucas për gjenerimin e mostrave të ARN-së. Ne falenderojmë më tej punonjësit e serave të Unifarm të Universitetit Solynta dhe Wageningen për ndihmën e tyre në mirëmbajtjen e bimëve dhe nxjerrjen e farës. Ky projekt ka marrë mbështetje financiare nga Organizata Holandeze e Kërkimeve Shkencore (Grant ID: NWA.17.023).
Kontributet e autorit
E.-JE projektoi dhe ekzekutoi eksperimentet dhe shkroi dorëshkrimin. AvdB projektoi dhe ekzekutoi qasjet WGS, KASP dhe bioinformatikë. SvH, RGFV, CWBB, MEdV dhe PL ndihmuan në hartimin e qasjes për studimet e hartës gjenetike dhe karakterizimin funksional të Rrëshqitje. RGFV, CWBB dhe PL rishikuan dhe komentuan dorëshkrimin.
I(S) Q) Qasja e hapur Ky artikull është i licencuar nën një licencë Creative Commons Attribution 4.0 International, e cila lejon përdorimin, ndarjen, adaptimin, shpërndarjen dhe riprodhimin në çdo medium ose format, për sa kohë që ju i jepni kredi të përshtatshme autorit / ëve origjinal dhe burimit, siguroni një lidhje me licencën Creative Commons dhe tregoni nëse janë bërë ndryshime. Imazhet ose materiali tjetër i palës së tretë në këtë artikull përfshihen në licencën e artikullit Creative Commons, përveç nëse tregohet ndryshe në një linjë kredie për materialin. Nëse materiali nuk është i përfshirë në licencën Creative Commons të artikullit dhe përdorimi juaj i synuar nuk lejohet me rregullore ligjore ose tejkalon përdorimin e lejuar, do t'ju duhet të merrni leje direkt nga mbajtësi i të drejtave të autorit. Për të parë një kopje të kësaj licence, vizitoni http://creativecommons.org/ licenca/nga/4.0/.









